Introduksjon:
Rubidiumoksid er et uorganisk stoff med viktige kjemiske og fysiske egenskaper. Oppdagelsen og forskningen på det har spilt en viktig rolle i å fremme utviklingen av moderne kjemi og materialvitenskap. I løpet av de siste tiårene har mange forskningsresultater om rubidiumoksid ikke bare fremmet fremskritt på dette feltet, men har også blitt mye brukt i andre relaterte felt, som halvledermaterialer, optikk, biomedisin, osv. Derfor,UrbanGruveteknologi.Co., Ltd., som en ledende bedrift i Kina som fokuserer på forskning, utvikling og produksjon av rubidiumoksidprodukter, har ekstremt viktig praktisk betydning for å utforske den kjemiske strukturen, fysiske egenskapene og anvendelsesmulighetene til rubidiumoksid grundig.
Kjemisk egenskapskarakterisering:
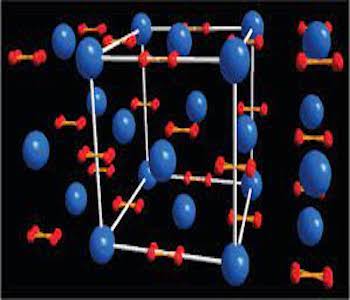
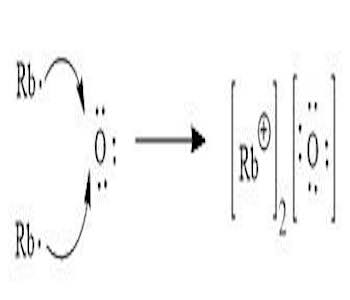
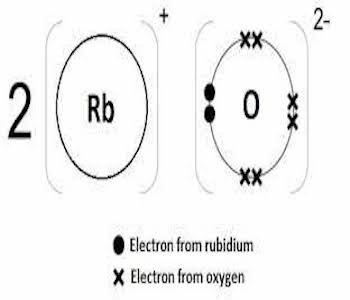
Rubidiumoksid (Rb2O)er et oksid av rubidium med den kjemiske formelen Rb2O, hvor oksidasjonstilstanden til oksygen er -2 og oksidasjonstilstanden til rubidium er +1. Denne forbindelsen er et alkalioksid, svært kjemisk aktivt og lett løselig i vann og mange organiske løsemidler. I tillegg er rubidiumoksid også svært reaktivt og kan reagere raskt når det møter sure stoffer og produsere noen nøytrale eller alkaliske stoffer. De kjemiske egenskapene til rubidiumoksid er også mye brukt på mange felt. For eksempel brukes det i metallurgisk industri som et viktig flussmiddel for høytemperaturfremstilling (eller reduksjon) av rubidiummetall; det er også mye brukt i fremstilling av forskjellige beleggfrie alkalier, opasifikatorer og tørkemidler; i tillegg brukes det også i produksjon av kaliumgjødsel. Bredt bruksområde.
Karakterisering av fysiske egenskaper:
De fysiske egenskapene til rubidiumoksid har også fått bred oppmerksomhet. Når det gjelder fysiske egenskaper, er rubidiumoksid en type uorganisk forbindelse med viktige elektriske, magnetiske og optiske egenskaper. Blant dem er elektriske egenskaper en av de viktigste fysiske egenskapene, og de har blitt mye brukt i halvlederenheter, optoelektroniske enheter og andre felt. Karakterisering av elektriske egenskaper Rubidiumoksid er en halvleder med ekstremt lav konduktivitet. Dens konduktivitet ved normal temperatur og trykk er svært lav, omtrent 10^-10 (S/m). Derfor krever studiet av elektriske egenskaper bruk av passende temperatur og trykk. Når temperaturen stiger til bare noen få hundre grader, kan dens elektriske konduktivitet forbedres betydelig. For eksempel, når temperaturen når 500°C, dens elektriske ledningsevne kan stige til 10^-7 (S/m), noe som gjør det lettere å lede elektriske egenskaper. Forskning. Magnetiske egenskaper til rubidiumoksid Den magnetiske susceptibiliteten til rubidiumoksid vil endre seg under påvirkning av et magnetfelt over lang tid. Derfor, under påvirkning av et langsiktig magnetfelt, kan magnetismen til rubidiumoksid endre seg i én retning. Dette fenomenet kalles magnetfelteffekten av magnetiseringskurven. Ved en viss temperatur kan denne effekten brukes til å studere de magnetiske egenskapene til materialer.
Søknadsmuligheter:
Rubidiumoksid har brede anvendelsesmuligheter som en uorganisk forbindelse. For eksempel, når det gjelder oksygensensorer, har de fleste studier funnet at rubidiumoksid-nanopartikler har utmerket respons i oksygenmåling; innen giftdeteksjon, biomedisin og hydrologi fungerer det som en viktig ligand og probeforbindelse. Det har blitt mye brukt; i tillegg forventes rubidiumoksid også å spille en viktig rolle innen energisparende materialer og forurensningskontroll, spesielt i atmosfærisk miljøvern. Bruken av rubidiumoksid kan være et effektivt middel for å bekjempe luftforurensning.
Konklusjon Generelt:
RUbidiumoksid er et uorganisk stoff med høy aktivitet og viktige anvendelsesmuligheter. Forskning på dets kjemiske egenskaper, fysiske egenskaper og anvendelsesmuligheter vil spille en viktig rolle i å fremme utviklingen av moderne kjemi og materialvitenskap. Derfor er det, samtidig som grunnforskningen styrkes, nødvendig å øke anvendelsen og utviklingen av rubidiumoksid på ulike felt og ytterligere fremme utviklingen og innovasjonen av dets tverrfaglige anvendelser.